Cell重大研究新突破:找到T细胞耗竭背后的核心元凶
本文来自微信公众号:生物世界,编辑:王多鱼,作者:生物世界
作为免疫系统里负责防御的核心力量,T细胞的抗癌能力并非无限。在肿瘤持续存在的微环境中,长期接触抗原刺激的T细胞往往会进入功能衰退的耗竭状态,失去杀伤癌细胞的能力,这也是很多癌症治疗效果不佳的关键原因之一。如何让耗竭的T细胞恢复功能,是当下癌症免疫治疗领域最重要的研究方向之一。
近日发表在顶级期刊Cell上的一项全新研究,找到了引发T细胞耗竭的一个此前未被关注的核心因素。
加州大学圣地亚哥分校的研究团队完成了这项研究,相关研究论文以《蛋白质稳态维持T细胞分化潜能与肿瘤浸润淋巴细胞功能》为题发表在Cell期刊上。
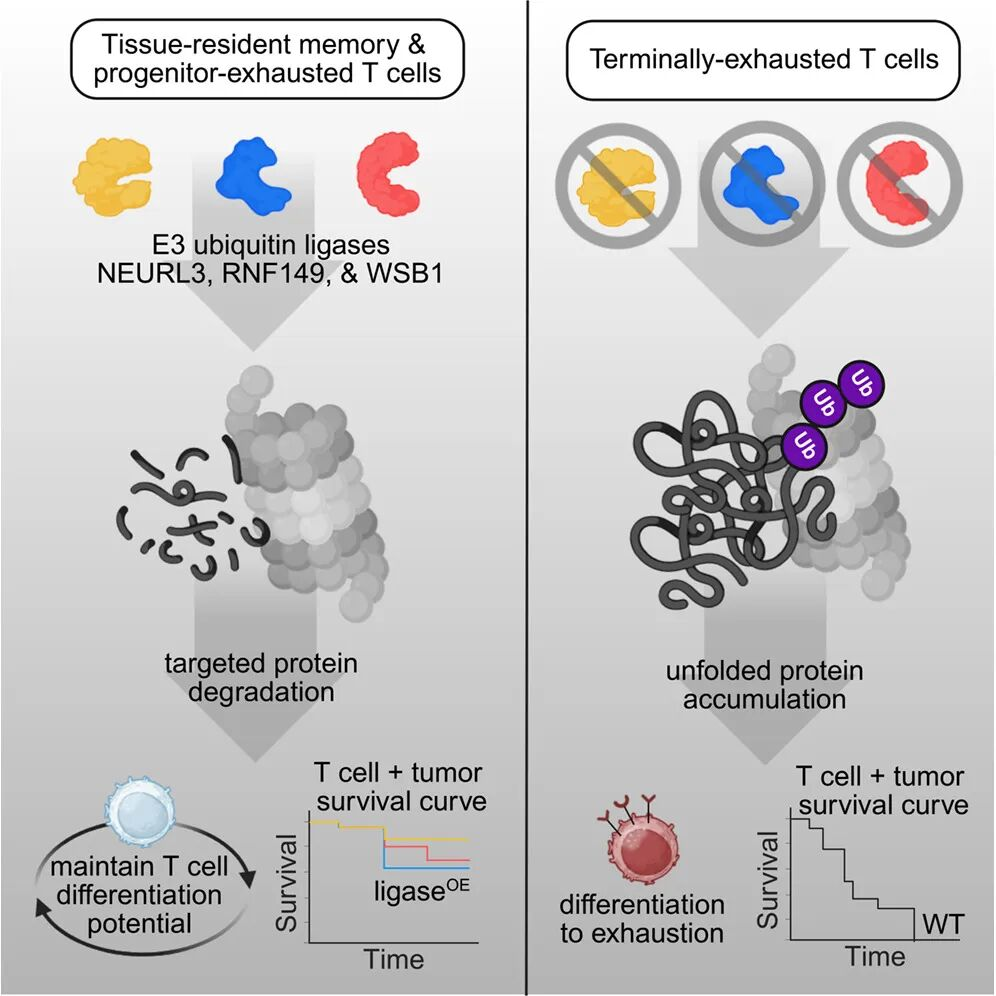
该研究明确指出:细胞内蛋白质稳态的丧失,才是导致T细胞进入耗竭状态的核心元凶;蛋白质稳态本身是维持T细胞分化潜能、保障肿瘤浸润淋巴细胞功能的关键基础,而通过E3泛素连接酶重建蛋白质稳态,能够有效提升机体对癌症免疫治疗的响应效果。

在肿瘤内部的肿瘤浸润淋巴细胞(TIL),往往会随着刺激时间推移逐步进入耗竭状态,无法有效抑制肿瘤进展。与之相比,组织驻留记忆T细胞(TRM)在初次接触抗原后,能在健康组织中长期停留,维持数年的免疫防护能力。临床数据显示,如果癌症患者的肿瘤中存在带有TRM特征的肿瘤浸润淋巴细胞,这类患者的预后效果通常会更好。
什么是蛋白质稳态?它是细胞内一整套调控蛋白质正确合成、转运、降解的协同调控网络,其中蛋白质回收是这个网络的关键环节:健康细胞会持续分解老旧、受损的异常蛋白质,在节省能量的同时,重新利用氨基酸等原料合成新的功能蛋白。
在本次研究中,研究团队对不同状态的T细胞群体同时做了蛋白质组和转录组分析,结果发现蛋白质稳态是区分不同功能T细胞的核心标志:终末耗竭的肿瘤浸润淋巴细胞,会丢失NEURL3、RNF149、WSB1这三种E3泛素连接酶,最终导致未折叠的异常蛋白质不断在细胞内累积——哪怕负责降解蛋白质的蛋白酶体本身功能是正常的。E3泛素连接酶是细胞内蛋白质降解调控体系的核心,它的作用就是给需要降解回收的蛋白质打上标记,引导细胞完成降解过程,当这些酶在终末耗竭T细胞中停止工作,本该被清理的蛋白质就会异常堆积,引发细胞功能紊乱。
研究团队进一步通过功能实验验证了这一发现:如果在T细胞中强制表达这几种E3泛素连接酶,就能有效维持TCF1阳性干细胞样T细胞群体的比例,显著提升T细胞在肿瘤模型和慢性感染模型中的杀伤功能;反过来,如果敲除这些E3泛素连接酶,就会损伤肿瘤浸润淋巴细胞的功能,还会改变急性感染过程中T细胞的正常分化过程。实验结果显示,持续维持E3泛素连接酶的表达,可以有效清除终末耗竭T细胞中累积的未折叠蛋白,还能在临床前肿瘤模型中显著改善免疫治疗的效果。
这项新发现明确了蛋白质稳态对维持肿瘤浸润淋巴细胞功能的核心作用,为开发新一代癌症免疫治疗开辟了全新的方向。此外,研究团队也指出,蛋白质稳态丧失并不是T细胞耗竭独有的特征,很多和异常蛋白质堆积相关的疾病,比如帕金森病、阿尔茨海默病这类神经退行性疾病,这项发现也可能带来全新的研究思路和治疗启发。
本文仅代表作者观点,版权归原创者所有,如需转载请在文中注明来源及作者名字。
免责声明:本文系转载编辑文章,仅作分享之用。如分享内容、图片侵犯到您的版权或非授权发布,请及时与我们联系进行审核处理或删除,您可以发送材料至邮箱:service@tojoy.com







