工程化细胞:mRNA精准递送的可编程新载体
本文源自微信公众号RNAScript,作者一一,原标题为《工程化细胞作为可编程的mRNA递送载体》
mRNA疗法发展初期,脂质纳米颗粒(LNP)虽实现了技术突围,但本质上只是“勉强够用”。静脉注射后,大部分剂量集中在肝脏,若想精准递送至肺、脑或实体瘤微环境,难度极大;要让mRNA仅进入预设靶细胞、实现零脱靶,更是难上加难;而若期望药效持续稳定,避免随注射次数衰减,几乎没有解决办法。
过去几年,行业为优化LNP配方投入大量研发资源,技术迭代从未停止,然而肝外递送效率低、细胞靶向性差、作用时长受限等核心瓶颈,始终难以突破,已触及明显的技术天花板。
就在行业受困于LNP迭代瓶颈之际,Arc研究所与加州理工学院的Felix Horns、Michael Elowitz(合成生物学领域权威专家)团队,在《Nature Reviews Bioengineering》发表了题为“Engineered cells as programmable mRNA delivery vehicles”的评论文章,提出了一个具有方向性的问题:若不再改良“包裹”方式,而是彻底更换配送体系——用工程化细胞替代LNP,让细胞本身成为可编程的mRNA精准递送载体,结果会如何?
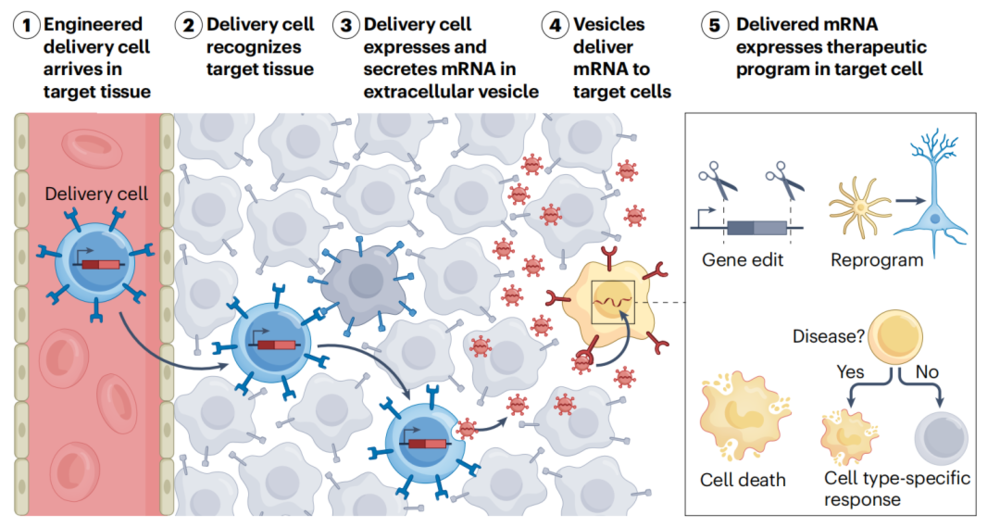
自然界的细胞RNA递送机制提供灵感
这一构想并非凭空而来,自然界早已将细胞间的RNA递送写入多细胞生物的底层通讯规则,只是此前未被真正工程化、工具化。
免疫细胞可通过免疫突触交换微小RNA(microRNA),实现免疫信号的协同传递;
神经元能借助Arc蛋白(一种由“驯化”的逆转录转座子编码的蛋白),将mRNA打包进病毒样颗粒,完成神经细胞间的跨细胞传递;
寄生线虫甚至能向哺乳动物宿主细胞分泌携带小RNA的外泌体,精准调控宿主的先天免疫应答。
在亿万年演化形成的细胞通讯网络中,RNA的跨细胞转移本就是成熟的生理功能,只需通过工程化改造,即可实现可控的规模与精度。
实际上,Horns团队早在2023年《Cell》发表的研究“Engineering RNA export for measurement and manipulation of living cells”中,就已完成核心技术的初步验证:通过工程化改造,可将目标mRNA定向打包进胞外囊泡并实现跨细胞递送。无论是将RNA结合结构域与囊泡富集蛋白融合,还是利用病毒包装序列将特定mRNA装载进工程化颗粒,核心技术路径均已打通。而这篇评论文章正是在此基础上,为整个领域描绘了一套完整的临床应用蓝图。
“递送细胞”的四层核心设计逻辑
这套“活体递送细胞”的核心设计,是将活细胞改造为具备环境感知、定向迁移、按需分泌能力的可编程mRNA递送系统,其核心逻辑分为四层,每一层都精准针对LNP的核心短板。
第一层是天然的靶向归巢能力。不同细胞自带演化赋予的组织迁移与定位能力:
造血干细胞可精准归巢至骨髓;
间充质干细胞会主动趋向损伤组织;
单核细胞则能被高效招募至实体瘤微环境。
借助细胞本身的天然迁移能力,直接避开了LNP难以突破的组织屏障与递送效率问题。
第二层是条件性的识别与激活。递送细胞可通过工程化改造搭载合成受体,只有感知到靶组织的特异性抗原、细胞因子或其他特征信号时,才会启动mRNA的表达与分泌。这使mRNA递送成为“时空可控”的精准行为——仅在正确的位置、正确的时机启动,从源头大幅降低脱靶毒性。
第三层是长效的持续递送能力。LNP属于典型的“一次性给药”,注射后便进入代谢衰减周期,蛋白表达完全受药代动力学曲线限制。而递送细胞可在靶位点持续产生携带mRNA的胞外囊泡,长期维持局部治疗性mRNA的有效浓度,完全突破了单次给药的剂量限制,在需要长期蛋白表达的适应症中具有天然的逻辑优势。
第四层是可控的安全终止机制。与CAR-T细胞的工程化逻辑一致,递送细胞可内置增殖调控模块与自杀开关(kill switch),在完成治疗任务或出现异常风险时,可被精准、可控地清除,保障临床安全底线。
三大高价值落地场景
在文章描绘的应用蓝图中,有三大场景最有可能率先实现突破,成为该技术的落地切入点。
第一个核心场景是体内基因编辑。大型基因编辑工具(如Cas9、先导编辑系统)或多组分编辑复合物的编码mRNA,往往超出LNP的装载上限;而递送细胞可同时传递多条mRNA,完美突破装载限制,还能实现LNP无法触及的深层组织的高效递送,大幅提升基因编辑的覆盖范围与效率。
第二个高价值场景是实体瘤治疗。单核细胞本身具备天然的肿瘤微环境趋化能力,若将其工程化为递送细胞,可在肿瘤原位持续分泌编码杀伤蛋白、免疫调节因子的mRNA,直接重塑肿瘤微环境,为实体瘤治疗提供了一条避开CAR-T浸润难题的全新路径。
第三个关键场景是再生医学。无论是将胰腺α细胞重编程为分泌胰岛素的β细胞以治疗糖尿病,还是在神经损伤部位原位诱导胶质细胞向神经元转分化,都需要在靶组织内长期、稳定表达特定转录因子。这种需求恰恰是固定剂量LNP难以满足,却是递送细胞的天然优势所在。
从概念到临床需跨越的四道门槛
值得肯定的是,作者在文章中并未回避该技术的核心挑战,这也是这篇评论文章优于空泛愿景文章的核心价值——它清晰列出了从概念走向临床必须跨越的四道核心门槛。
第一道是免疫原性难题。目前胞外囊泡的mRNA分泌系统大多整合了非人源的蛋白结构域(如病毒包装蛋白),不仅系统组件本身可能引发免疫反应,工程化的递送细胞也存在触发宿主免疫排斥的风险。如何设计全人源化的功能组件,是必须攻克的首要工程难题。
第二道是归巢能力的泛化性瓶颈。目前可利用的归巢机制均为特定细胞类型的天然属性,缺乏一套通用、可编程的“细胞导航”工具。不同的靶器官、不同的肿瘤类型可能需要完全不同的递送细胞底盘,这将大幅增加规模化开发的成本与难度。
第三道是递送特异性的可控性挑战。尽管原理上可通过多层工程设计实现靶向递送,但在实际生理环境中,胞外囊泡的分泌与摄取无法做到100%受控。靶标特异性的实现需要多层基因回路的叠加,系统复杂度越高,潜在的失控风险也会同步上升。
第四道是产业化与监管的双重壁垒。活细胞药物本身就处于监管的高门槛地带,而递送细胞比已获批的CAR-T产品多了一层“持续分泌生物活性囊泡”的复杂性。如何界定给药剂量、如何评估长期安全性窗口、如何建立标准化的生产工艺,目前均无成熟框架可循。
mRNA递送技术进入新战场
为何这一方向在当下值得全行业认真关注?
并非因为构想新颖,而是其出现的时间点恰好处于技术成熟的临界点:近三年,合成受体(如synNotch系统)、RNA感应基因回路、可编程胞外囊泡的工程化工具箱已完成关键技术积累。2025年,同一团队发布的癌症治疗合成蛋白回路预印本,更证明这套工程化逻辑已从概念构想进入实验验证阶段。
更核心的行业驱动力来自mRNA领域的真实痛点:LNP平台在肝外递送的商业化瓶颈已转化为巨大的未被满足的技术需求。谁能在下一代递送范式上完成早期专利布局与工程化积累,谁就能掌握后mRNA时代的技术话语权——而Horns与Elowitz团队早已通过加州理工学院提交了相关技术的专利申请。
当然,在相当长的时间里,工程化递送细胞都不会成为mRNA递送的“通用解决方案”。它最有可能率先落地的场景,恰恰是LNP完全无能为力的细分领域:难以抵达的深层组织、需要长期稳定表达的蛋白疗法、需要原位精准激活的体内基因编辑任务。
mRNA疗法的核心瓶颈从来都不只是核酸化学问题。这场关于递送的战争,已从材料配方优化进入活细胞工程化设计的全新战场。
本文仅代表作者观点,版权归原创者所有,如需转载请在文中注明来源及作者名字。
免责声明:本文系转载编辑文章,仅作分享之用。如分享内容、图片侵犯到您的版权或非授权发布,请及时与我们联系进行审核处理或删除,您可以发送材料至邮箱:service@tojoy.com




