Nature子刊新研究:阻断mRNA疫苗在肝脏表达可提升免疫效果
本文来自微信公众号:生物世界,编辑:王多鱼,作者:生物世界
由mRNA疫苗编码的蛋白质,可以在被转染的多种不同细胞中合成表达。目前常用的脂质纳米颗粒(LNP)递送系统,会让mRNA在进入人体后更容易向肝脏富集,然而,mRNA在不同细胞中的特异性表达究竟会对机体免疫应答产生怎样的影响,这个问题到现在依旧没有明确答案。
2026年4月29日,美国西奈山伊坎医学院的研究团队在顶级期刊Nature Biotechnology发表了一篇研究论文,论文标题为:mRNA vaccine immunity is enhanced by hepatocyte detargeting and not dependent on dendritic cell expression。
这项研究得到了一个十分重要的结论:如果让mRNA疫苗不再靶向肝细胞,不让抗原在肝细胞中表达,能够显著提升mRNA癌症疫苗的免疫效果;而且疫苗激活人体免疫应答的过程,并不需要专职抗原呈递细胞树突状细胞表达抗原。

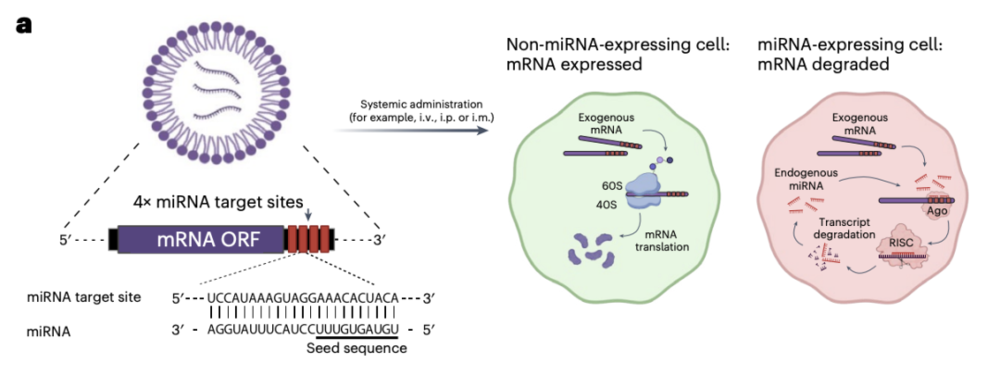
在本次研究中,研究团队开发了一种全新的调控策略:在脂质纳米颗粒(LNP)递送的mRNA疫苗上,插入人工合成的microRNA靶位点(miRT),通过这个设计,可以特异性地让特定细胞中的mRNA沉默,也就是阻止这些细胞翻译表达mRNA编码的抗原。在实验中,研究团队分别沉默了专职抗原呈递细胞(pAPC,也就是树突状细胞这类细胞)、肝细胞以及肌细胞的mRNA表达,来验证不同细胞表达抗原对免疫激活的作用。
研究得到了三项核心发现:
1、专职抗原呈递细胞表达抗原,并不是激活抗原特异性T细胞必不可少的条件;
2、如果只让肌细胞表达mRNA编码的抗原,能够诱导出强度相当甚至更强的免疫应答,这其中也包含针对新冠病毒SARS-CoV-2的免疫应答。这个结果说明,抗原交叉呈递或者交叉着装的效应,可能比专职抗原呈递细胞自己表达抗原对免疫激活的作用更大;
3、如果让肝细胞表达mRNA编码的抗原,反而会抑制抗原特异性T细胞的免疫应答,进一步研究发现,这个抑制作用部分是通过PD-1/PD-L1通路实现的。
研究团队又在携带淋巴瘤(淋巴瘤细胞表达肿瘤相关抗原TAA)的小鼠模型上做了验证,结果显示,利用miRT技术沉默肝细胞的抗原表达后,mRNA疫苗诱导出了更强的抗肿瘤免疫应答,小鼠体内的肿瘤负荷也明显更低。这个实验证实,非专职抗原呈递细胞的抗原表达,确实可以调控机体对mRNA编码蛋白的免疫应答,在mRNA疫苗中引入miRT,可以定向调控mRNA-LNP的免疫原性,增强或者削弱免疫反应。
这项研究推翻了两个领域内的传统认知——
1、过去学界普遍认为,树突状细胞作为专职抗原呈递细胞,直接摄取mRNA、表达抗原,是启动T细胞免疫的关键环节。但这项研究显示,其实更主要的途径是:树突状细胞不需要自己表达抗原,其他细胞比如肌细胞表达抗原之后,树突状细胞可以通过交叉呈递或者交叉着装捕获这些抗原,再把抗原提呈给T细胞,照样可以启动有效的免疫应答。
2、传统认知认为,疫苗递送的抗原在任何体细胞中表达,都对激活免疫有帮助。但这项研究却发现,mRNA在肝细胞中表达不仅没用,反而会抑制抗原特异性T细胞的免疫反应,只要关闭mRNA疫苗在肝细胞中的表达,就能明显让疫苗的免疫效果变强。
总的来说,这项研究改变了我们之前对mRNA疫苗作用机制的简单认知,还提出了一个优化疫苗设计的全新方向:通过精细调控mRNA在不同细胞中的特异性表达,就可以提升疫苗的免疫效力,开发出效果更好的mRNA疫苗。
本文仅代表作者观点,版权归原创者所有,如需转载请在文中注明来源及作者名字。
免责声明:本文系转载编辑文章,仅作分享之用。如分享内容、图片侵犯到您的版权或非授权发布,请及时与我们联系进行审核处理或删除,您可以发送材料至邮箱:service@tojoy.com







